一批新药将上市:恒瑞、东阳光、正大天晴...
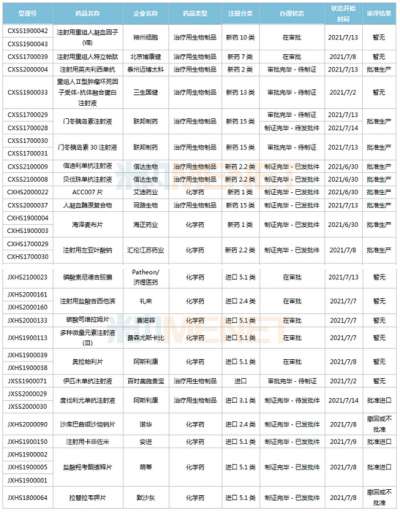
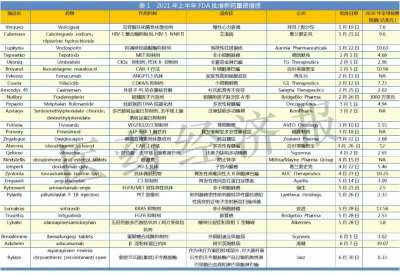
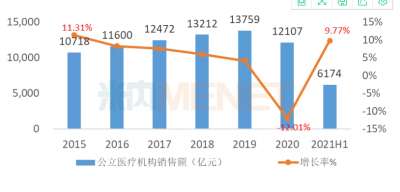
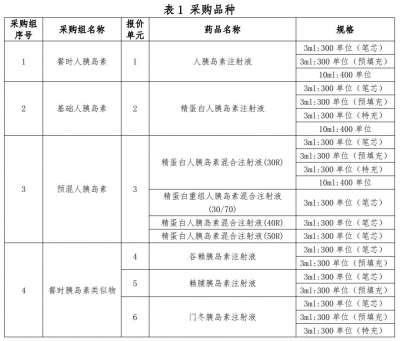
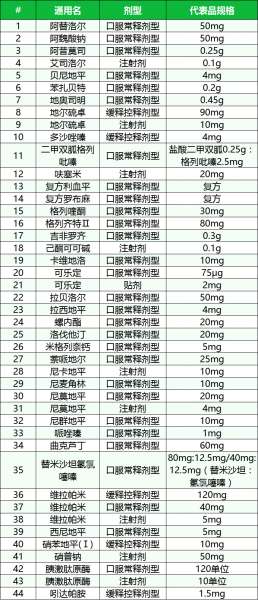
医药网7月20日讯 多款新药上市有新进展,国内外头部药企均有斩获 23款新药上市有进展!2款国产1类新药首次获批 6月26日-7月16日期间,23个新药(33个受理号)的上市申请有审评审批状态更新。9款国产新药获批上市,其中2款1类新药首次获批,包括艾迪药业的艾诺韦林片(曾用名ACC007片)、海正药业的海泽麦布片;3个新药获批进口,安进的注射用卡非佐米、萌蒂的盐酸羟考酮缓释片首次获批。 此外,神州细胞的注射用重组人凝血因子(Ⅷ)、北京博康健的注射用重组人特立帕肽、礼来的注射用盐酸吉西他滨、赛诺菲的碳酸司维拉姆片、阿斯利康的奥拉帕利片等7个药品的注册办理状态变更为“在审批”。 (6.26-7.16)新药上市申请审评审批状态更新 2款国产1类新药首次获批上市。海博麦布片是海正药业首个获批上市的1类新药,这是一款胆吸收抑制剂,用于治疗原发性高胆血症。同靶点上市药物为默沙东的依折麦布,全球销售峰值达26.6亿美元,2020年在中国城市公立、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)及中国城市实体终端合计销售额接近10亿元;艾诺韦林片(曾用名ACC007片)是全新结构的非核苷类逆转录酶抑制剂,是艾迪药业首个获批的抗艾滋病1类新药。 联邦制药2款胰岛素获批上市,均为国产第2家。门冬胰岛素注射液是一种速效的人胰岛素类似物,门冬胰岛素30注射液是由可溶性门冬胰岛素和精蛋白门冬胰岛素按30:70的比例组成的预混胰岛素。米内网数据显示,2020年中国公立医疗机构及中国城市实体药店终端胰岛素及其类似药销售规模超过300亿元。 首次在国内获批的注射用卡非佐米是百济神州/安进联合开发的一款蛋白酶体抑制剂,联合地塞米松治疗复发或难治性多发性骨髓瘤。该产品